骨形态学的研究非常重要,骨的完整性、脆弱性和机械性能高度依赖于骨结构和孔隙度,它们受到老化、骨质疏松、骨生成不完善、糖尿病、神经纤维瘤等疾病的影响。骨结构和形态的研究对于评估骨的机械性能和预测骨折风险具有重要意义,许多临床和研究在文献中对常规骨结构变化进行了广泛的研究[1]。
相比之下,关于骨小梁的变化(特别由年龄或疾病引起的形态变化)的数据有限,但这些都与骨质疏松症患者的骨脆性和骨折风险密切相关。许多文献报告表明,小梁骨的宏观和微观结构变化与骨质疏松症的发展、骨折风险和骨机械行为有关。单纯的骨密度并不能解释所有与年龄和骨质疏松度有关的骨脆性病例,因为还必须考虑骨的微观结构和化学成分。事实上,骨骼成分、孔隙度和微结构中的局部变化可能会影响骨骼的机械性能。此外,据观察,小梁骨结构对骨强度的影响比骨密度的影响更大。由于这些原因,准确检测小梁骨的微观结构变化可以提供有趣的临床视角,特别是在骨质疏松症患者中,用于研究骨质疏松症相关骨折风险[2]。
常规的检测分析技术包括X射线吸收仪(DEXA)和超声波检查,然而,这些方法的作用是有限的,因为它们不能提供定性和定量的形态学信息。低场核磁共振技术由于其在孔隙结构表征方面优秀的能力,已经成功地用于描述常规骨和小梁骨的孔隙度和形态特性[3.4]。
相比于高场核磁,低场核磁共振适用于更大的特征长度(从大约10纳米到500微米)的测试,由于这个原因,低场核磁共振很适合研究骨等多孔系统的结构。另一个不可忽视的优势是,与高场核磁共振相比,低场核磁共振设备的成本要低得多(通常是十分之一)。此外,低场核磁的维护成本和安全预防措施与高场核磁共振设备要低得多,也简单得多[5]。
实验目的:
测定骨孔隙中水质子的横向弛豫时间,以求得骨孔径分布,比较关节炎小梁骨和骨质疏松小梁骨的差异。
实验流程:(所有骨均为实验室中用于科学研究的样本)
1.从实验室收集15份50岁左右男性的股关节炎小梁骨样本,用于实验。
2.从实验室收集15份50岁左右男性的股骨质疏松小梁骨样本,用于实验。
3.采用特殊的取样装置获得直径6毫米、长度4毫米的骨圆柱体。
4.对样品进行清洗,放置在漂白剂中48小时。
5.然后在悬浮液中进行消毒,去除细胞成分。
6.在进行检测前对骨样本进行饱水,确保骨样本内部孔隙充满水。
7.将骨样本取出,擦拭表面的水分,用聚四氟乙烯材料对骨样本进行包裹,快速进行低场核磁共振测试,获得T2谱。
8.对测得的骨样本低场核磁共振信号,进行反演处理,对15份关节炎骨和15份骨质疏松骨进行平均计算,求得平均骨孔径分布。
9.对比关节炎骨和骨质疏松骨在核磁法中骨孔径分布的差异。
实验结果:
根据低场核磁共振测试结果,对共计三十分的样本进行取平均值处理,关节炎的骨平均孔隙度为74%,骨质疏松的骨平均孔隙度为78%。下图显示了不同骨孔隙尺寸对应的孔径分布。
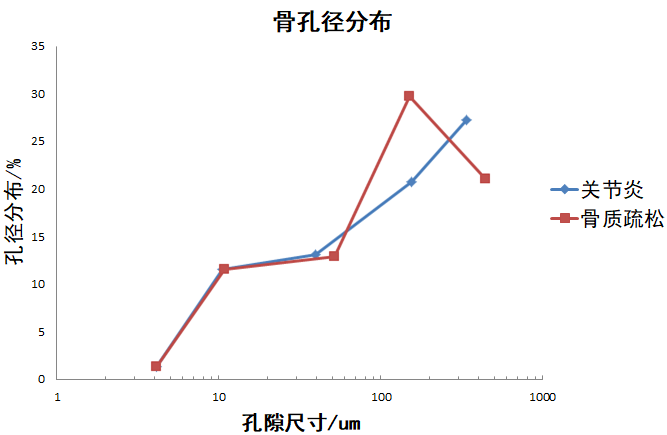
实验分析:
1)关节炎和骨质疏松作为常见骨类疾病的两种,二者在骨的总孔隙度上较为接近,骨质疏松的骨平均孔隙度稍大于关节炎的骨平均孔隙度,没有太大的差异。
具体的骨孔隙分布中显示:在1-60um的孔隙分布尺度上关节炎和骨质疏松的骨孔隙分布大致一致;在60-200um的孔隙分布尺度上,骨质疏松的骨孔径分布明显大于关节炎的骨孔隙分布;在200-1000um的孔隙分布尺度上,关节炎的骨孔径分布明显大于骨质疏松的骨孔隙度。二者的孔隙分布证明了,虽然两种骨类疾病的平均孔隙度较为接近,但是在低场核磁表征的骨孔隙尺寸分布上还是存在明显的差异。

NM21-015V-I(纽迈低场核磁生命科学领域设备)
如您对以上应用感兴趣,欢迎咨询:400-060-3233
参考资料
[1] Bakalova L P, Andreasen C M, Thomsen J S, et al. Intracortical Bone Mechanics Are Related to Pore Morphology and Remodeling in Human Bone[J]. Journal of Bone and Mineral Research, 2018, 33(12):2177-2185.
[2] Juan, Katherine, Brooke-Wavell, et al. Characterising variability and regional correlations of microstructure and mechanical competence of human tibial trabecular bone: An in-vivo HR-pQCT study.[J]. Bone, 2019.
[3] Rajapakse C S, Bashoor-Zadeh M, Li C, et al. Volumetric Cortical Bone Porosity Assessment with MR Imaging: Validation and Clinical Feasibility[J]. Radiology, 2015, 276(2):526-35.
[4] Wurnig, M.C, Calcagni, M, et al. Characterization of trabecular bone density with ultra-short echo- time MRI at 1.5, 3.0 and 7.0 T–comparison with micro-computed tomography. NMR Biomed[J]. 2014, 27, 1159–1166.
[5] Abrami M, Chiarappa G, Farra R, et al. Use of low-field NMR for the characterization of gels and biological tissues[J]. ADMET & DMPK, 2018, 6(1):34.
电话:400-060-3233
售后:400-060-3233


返回顶部